Enzym spielt eine wichtige Rolle: Wie Leberkrebs entsteht
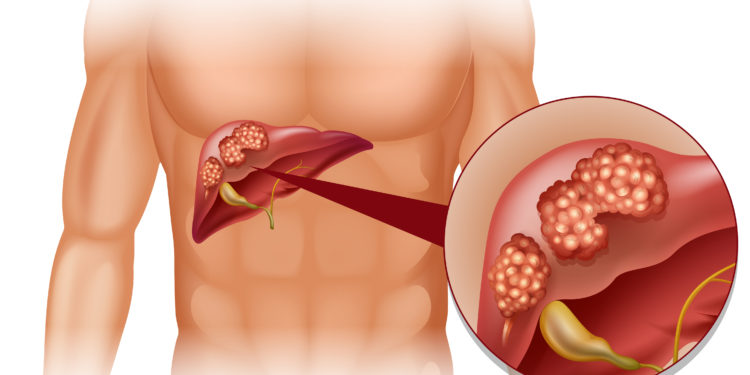
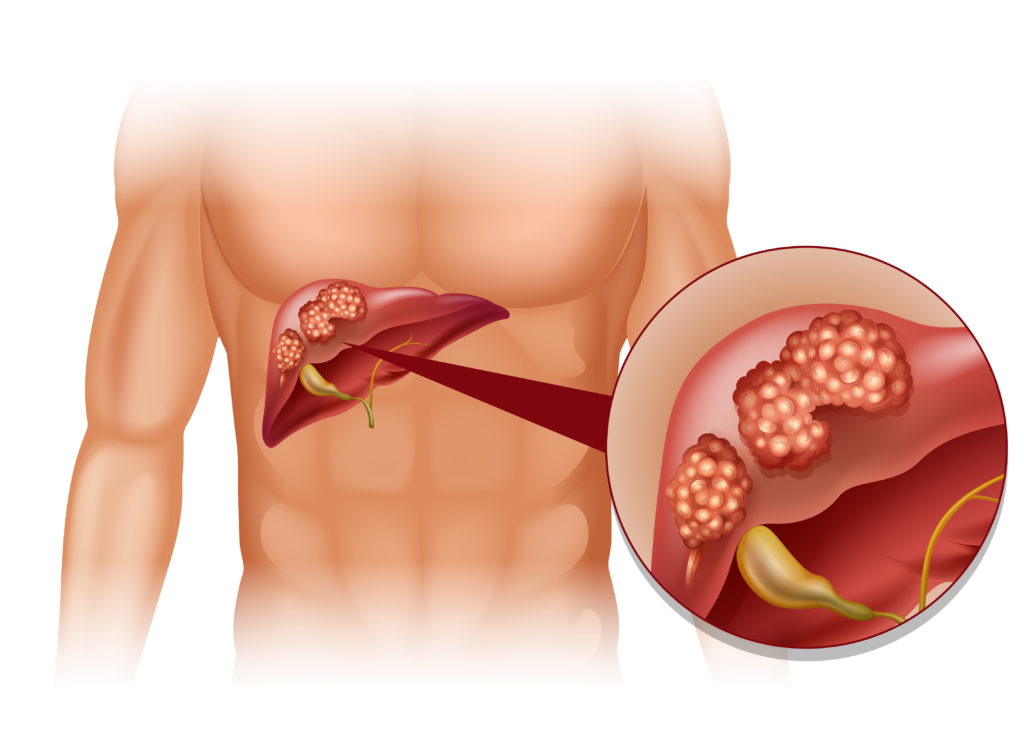
Leberkrebs ist weltweit die zweithäufigste krebsbedingte Todesursache und jene Krebserkrankung, deren Häufigkeit am schnellsten zunimmt. Forscher haben nun einen zentralen Mechanismus entdeckt, wie Leberkrebs entsteht. Die neuen Erkenntnisse sind unter anderem für die Behandlung von Patienten mit chronischen Lebererkrankungen von Bedeutung.
Zweithäufigste krebsbedingte Todesursache
Gesundheitsexperten zufolge ist Leberkrebs weltweit die zweithäufigste krebsbedingte Todesursache und jene Krebserkrankung, deren Häufigkeit am schnellsten zunimmt. Ein internationales Forscherteam hat nun einen zentralen Mechanismus entdeckt, wie Leberkrebs entsteht. Ein bestimmtes Enzym spielt dabei eine wichtige Rolle.
Leberkrebs durch chronische Lebererkrankungen
In den meisten Fällen entwickelt sich der Tumor bei Patienten mit chronischen Lebererkrankungen. Da Leberkrebs und Leberzirrhose häufig auf chronische Infektionen mit Hepatitis-Viren zurückzuführen sind, fordern Mediziner immer wieder Routinetests, um die verborgenen Ansteckungen aufzuspüren.
Das Risiko für Leberkrebs erhöht sich auch durch eine sogenannte Fettleber, die beispielsweise auf ernährungsbedingte beziehungsweise genetisch verursachte Fettstoffwechselstörungen oder übermäßigen Alkoholkonsum zurückgeht.
US-amerikanische Wissenschaftler veröffentlichten im vergangenen Jahr zudem eine Studie, die Hinweise darauf lieferte, dass Adipositas und Typ-2-Diabetes das Risiko von Leberkrebs erhöhen.
Zelltod begünstigt Tumorentstehung
Obwohl seit längerem bekannt ist, dass Leberzellkrebs besonders häufig entsteht, nachdem die Leber durch chronische Krankheit geschädigt worden ist, war bisher unklar, wie diese Ereignisse auf molekularer Ebene zusammenhängen.
Ein internationales Team von Wissenschaftlern vom Deutschen Krebsforschungszentrum (DKFZ) und von der Universität Zürich (UZH) hat jetzt gezeigt, dass chronischer Zelltod die Tumorentstehung begünstigt.
Je mehr Zellen absterben, desto stärker müssen sich die verbliebenen Zellen teilen. Bei diesen Teilungen häufen sie Mutationen an: ein Nährboden für Leberzellkrebs, schreibt das DKFZ in einer Mitteilung.
Enzym nimmt eine wichtige Doppelrolle ein
Die Wissenschaftler stellten fest, dass das Enzym Caspase 8 bei diesem Prozess eine wichtige Doppelfunktion einnimmt. Die Untersuchungen fanden zunächst an Mäusen statt. Patientendaten zeigen, dass die Ergebnisse auf den Menschen übertragbar sind.
Einerseits ist Caspase 8 wichtig für den programmierten Zelltod, Apoptose genannt. Durch Apoptose schützen entartete Zellen den Organismus, indem sie sich selbst eliminieren. Lange Zeit galt deshalb das Motto: Apoptose schützt vor Krebs.
Die aktuelle Studie, die im Fachmagazin „Cancer Cell“ veröffentlicht wurde, zeigt, dass das nur für jede einzelne Zelle gilt, nicht aber für das gesamte Gewebe der Leber.
Mutationen in der DNA
Unterlaufen zu viele Zellen gleichzeitig eine Apoptose, begünstigt das die Krebsentstehung. Der Grund: Die verbleibenden Leberzellen müssen sich dann viel stärker teilen, um den Gewebeverlust auszugleichen.
„Leberzellen sind so hohe Teilungsraten über einen längeren Zeitraum nicht gewöhnt, sie sind damit überfordert und machen Fehler“, erklärt Mathias Heikenwälder vom DKFZ in Heidelberg.
Patienten mit einer chronischen Leberentzündung akkumulieren daher zahlreiche DNA-Schäden – den Nährboden für Krebs.
Denn je mehr Mutationen sich in die DNA einschleichen, desto wahrscheinlicher ist es, dass die Zelle aus ihrem normalen Lebenszyklus ausbricht und sich ungehindert teilt und wächst.
Schäden erkennen und reparieren
Caspase 8 hat jedoch noch eine ganz andere Funktion. Das Molekül ist als Teil eines neu identifizierten, größeren Komplexes daran beteiligt, Schäden an der DNA zu erkennen und deren Reparatur einzuleiten.
Die Apoptose- und die Reparatur-Funktion arbeiten unabhängig voneinander. Sie lassen sich also auch getrennt voneinander beeinflussen.
Das ist besonders wichtig für die Behandlung von Leberkrebs oder chronischen Lebererkrankungen. Eliminierte man das Enzym Caspase 8 komplett, dann würde man zwar den programmierten Zelltod und die Entstehung von Krebs verhindern.
Gleichzeitig würde man die Zelle jedoch auch eines DNA-Reparaturmechanismus berauben. Das gilt es zu vermeiden.
Wichtig für die Behandlung von Patienten mit Lebererkrankungen
Als nächstes möchten die Wissenschaftler prüfen, ob es ähnliche Vorgänge auch bei anderen Krebsarten gibt und die Dynamik des Mechanismus genauer untersuchen.
„Wir wissen bisher nicht, wann und warum Caspase 8 und die anderen Moleküle sich zusammentun und nach DNA-Schäden suchen“, so Heikenwälder. „Da sind noch viele Fragen offen.“
UZH-Professor Achim Weber vom Institut für Pathologie und Molekularpathologie des Universitätsspitals Zürich erklärte in einer Mitteilung, dass die Ergebnisse der Studie aber nicht nur für die Grundlagenforschung relevant sind:
„Unsere Ergebnisse haben wichtige Implikationen für die Klinik – einerseits für die Behandlung von Patienten mit chronischen Lebererkrankungen und andererseits für die Anwendung Zelltod-induzierender Krebsmedikamente.“ (ad)
Autoren- und Quelleninformationen
Wichtiger Hinweis:
Dieser Artikel enthält nur allgemeine Hinweise und darf nicht zur Selbstdiagnose oder -behandlung verwendet werden. Er kann einen Arztbesuch nicht ersetzen.